🧬 단백질 공장이 암의 약점이다
암세포는 빠르게 분열하기 위해 대량의 단백질을 필요로 하며, 이를 위해 **리보솜(Ribosome)**이라는 세포 내 단백질 생성 공장을 과활성화합니다. 이 리보솜의 기본 재료인 **리보솜 RNA(rRNA)**는 **RNA Polymerase I (Pol I)**이라는 효소가 생성하는데, 이는 암세포에서 과활성화된 상태로 존재하는 경우가 많습니다. Johns Hopkins 연구진은 바로 이 Pol I을 억제하면 암세포에 비정상적 스트레스 반응을 유도하고, 나아가 암의 약점을 공략할 수 있는 치료 전략이 될 수 있다는 가능성을 보여주었습니다.
🔬 리보솜 구성 단백질 RPL22의 예상치 못한 이중 역할
리보솜의 구성 단백질인 RPL22가 단순한 구조 단백질이 아닌, RNA 스플라이싱 조절자로 작용한다는 사실이 밝혀졌습니다.
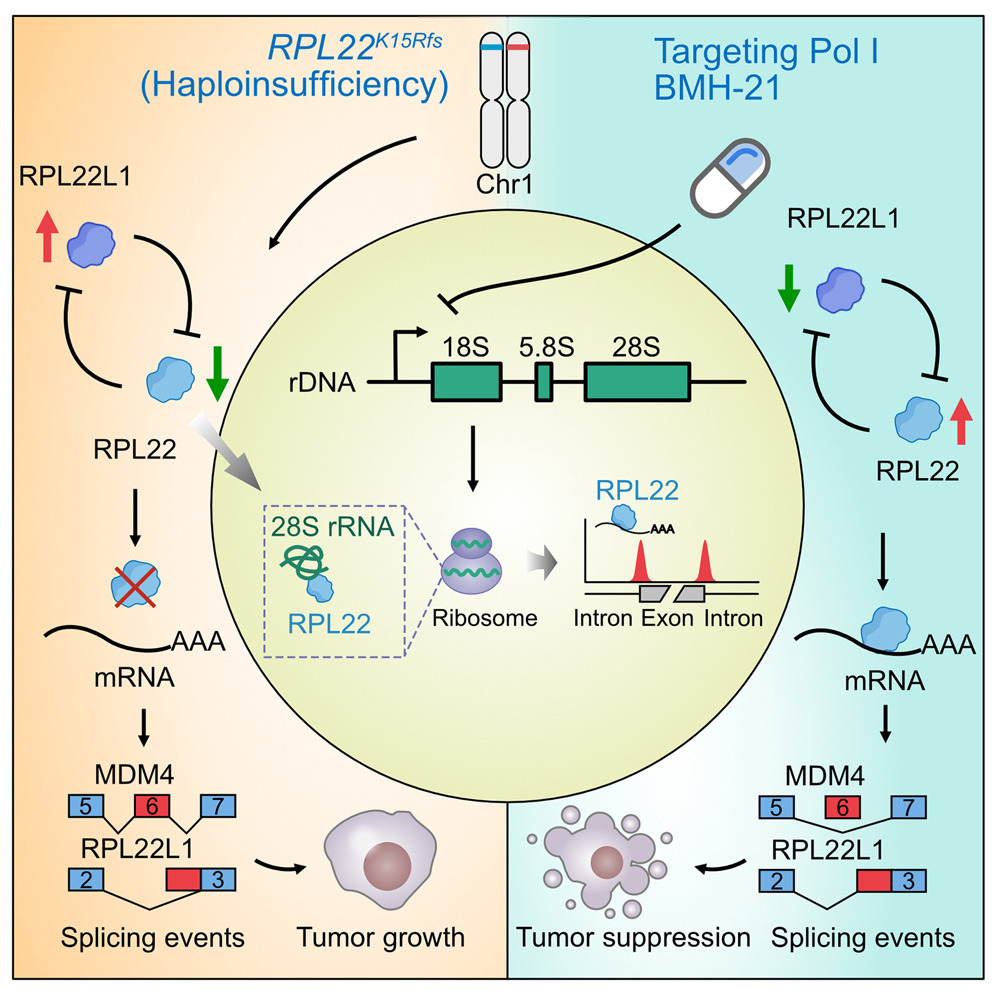
Pol I 억제제가 rRNA 생성을 막을 뿐 아니라, RPL22의 작용을 바꾸고, RNA 스플라이싱 방식 자체를 재설계하게 만드는 것입니다.
- RPL22는 원래 28S rRNA에 결합하지만,
- Pol I 억제 시, ribosome 밖으로 해방되어 mRNA 스플라이싱 조절에 관여
- 그 결과, MDM4 (p53 억제 단백질)와 RPL22L1 (암에서 과발현되는 유전자)의 스플라이싱과 발현 양상이 변화
🧪 특정 암에서 강력한 반응
연구진은 300개 이상의 암세포주를 대상으로 Pol I 억제제 BMH-21, BOB-42의 반응을 확인했고, 다음과 같은 유전적 특징을 가진 세포주가 민감하게 반응했습니다.
- RPL22 유전자 돌연변이 (K15Rfs hotspot)
- RPL22L1 과발현
- MDM4 단백질 과발현
이러한 특징은 MMR 결핍(MMRd) 암종에서 자주 나타나며, 이는 대장암, 위암, 자궁암 등에서 흔히 발견됩니다.
🧬 종양 억제 효과 최대 77%
- 흑색종, 대장암, 전립선암 모델에서 BOB-42는 종양 크기를 최대 77% 감소
- 환자 유래 종양(PDX) 모델에서도 75%까지 종양 성장 억제
- 치료는 독성 없이 잘 견디는 것으로 나타남 (체중 변화, 혈액 검사 정상)

🧩 RNA 스플라이싱 조절과 면역 인식
Pol I 억제는 단백질 생성을 억제할 뿐만 아니라, RNA 스플라이싱을 교란하여 **새로운 단백질 이소폼(isoform)**을 생성하게 만듭니다. 이는 종양이 면역계에 더 잘 인식되도록 유도할 수 있으며, 향후 면역항암제와 병용 전략으로 발전할 가능성을 시사합니다.
- 특히 MDM4-FL → MDM4-S로의 전환은 p53 억제 해제
- RPL22L1 variant 1 → variant 3 전환은 종양 성장 억제

📌 중요한 의의
- 암의 취약점(rRNA 생성)을 정밀하게 타겟팅하는 새로운 약물 전략을 제시
- RPL22 단백질이 스플라이싱 조절자로 기능함을 처음으로 규명
- Pol I 억제가 p53 의존성, 비의존성 경로를 동시에 활성화해 종양 억제 효과를 유도
- 향후 면역항암제와의 병용 가능성 및 치료 저항성 암을 겨냥한 전략으로 발전 가능
- MMRd 암에 대한 정밀 의료의 강력한 후보 표적 발굴
✍ 한줄평
“세포의 설계도를 바꾸면, 암은 생존할 수 없다—스플라이싱을 조절하라.”
참고논문 : DOI: 10.1101/2024.08.15.608201
'PaperReviews > Omics' 카테고리의 다른 글
| 암 전이의 비밀, 혈관에서 흘러나온 단서 - Shearosomes의 발견 (0) | 2025.07.13 |
|---|---|
| 비흡연자 폐암, 유전자에 새겨진 환경의 흔적 (0) | 2025.07.09 |
| 단일 세포 분석의 혁신: STAMP 기술로 100만 개 이상의 세포를 저렴하게! (0) | 2025.06.24 |
| 만성 신장 질환 환자의 코로나19: 면역 반응의 미묘한 차이를 파헤치다 (0) | 2025.06.23 |
| 유전자 설계의 새로운 지평: 전사 및 번역 조절의 비밀 밝히기 (0) | 2025.06.22 |